| فنی و مهندسی در این زیر تالار به بحث و گفتگو در مورد رشته های فنی و مهندسی پرداخته میشود |

11-11-2007
|
 |
مدیر کل سایت  کوروش نعلینی |
|
تاریخ عضویت: Jun 2007
محل سکونت: کرمانشاه
نوشته ها: 12,700
سپاسها: : 1,382
7,486 سپاس در 1,899 نوشته ایشان در یکماه اخیر
|
|
 شیمی و گرایشهای آن
شیمی و گرایشهای آن
شیمی و گرایشهای آن
شيمي علم اتمها، پيوندها و مولكولهاست. دانشي كه ميتواند خواص ماده، چگونگي تغييرات و شيوه توليد آنها را از هسته اتم گرفته تا كهكشانها بررسي كند و رشته شيمي، رشتهاي است كه به پرورش متخصصاني ميپردازد كه با مطالعه و تحقيق و آزمايش به ابداع و نوآوري پرداخته و يا فرآوردههاي شيميايي را كنترل ميكنند.
دكتر محمدحسين رفيعي استاد شيمي دانشگاه تهران در معرفي اين رشته ميگويد:
«رشته شيمي داراي دو بخش علم شيمي و صنايع شيمي است كه علم شيمي به عنوان يكي از علوم پايه زيربناي علوم مختلفي همچون بيولوژي ، بيوتكنولوژي ، پزشكي ، دندانپزشكي ، داروسازي و رشتههاي متعدد مهندسي است. اما صنايع شيميايي عبارت است از صنايعي كه در آنها واكنش شيميايي انجام ميگيرد يعني اقسام مواد اوليه تبديل به محصولات جديد ميگردد كه خواص اين محصولات تا حدودي با مواد اوليه متفاوت است.»
وي در ادامه ميگويد:
«با توجه به تعريف فوق صنايع شيمي طيف گستردهاي از صنايع را در بر ميگيرد كه از آن جمله ميتوان به صنايع غذايي، داروسازي، پتروشيمي ، الياف مصنوعي ، بهداشتي و آرايشي و صنايع توليد لوازم خانگي اشاره كرد.»
يكي ديگر از اساتيد دانشگاه در معرفي اين رشته ميگويد:
«بررسي و مطالعه اجمالي تركيب، ساختار و ويژگيهاي ماده و همچنين كنترل آزمايشگاهي فرآيندهاي شيميايي، مطالب و فعاليتهايي است كه در رشته شيمي در سطح كارشناسي ارائه ميگردد. در سطح كارشناسي ارشد و دكترا نيز دانشجويان در گرايشهاي تخصصي اين رشته كه عبارتند از : شيمي آلي ، شيمي تجزيه ، شيمي معدني ، شيمي فيزيك و شيمي كاربردي به صورت عميقتري با بخشي از علم شيمي آشنا ميگردند تا در آينده بتوانند مرزهاي دانش شيمي را گسترش دهند.»
تواناييهاي فارغالتحصيلان
فارغالتحصيلان اين دوره ميتوانند مسؤوليت زمينههاي مختلف از جمله موارد زير را عهدهدار باشند:
1- طرح، نظارت و اجراي طرحهاي تحقيقاتي كوچك و بزرگ شيميايي در سطوح مختلف كاربردي و علمي محض، در دانشگاهها، كارخانجات و مراكز تحقيقاتي ، به منظور ارتقاي كمي و كيفي محصولات مورد نياز جامعه .
2- مسووليت و ارائه خدمات در آزمايشگاههاي كنترل كيفي، پيگيري و ارائه معيارهاي استاندارد به منظور افزايش كميت و كيفيت محصولات توليدي و همچنين مواد مصرفي كارخانهها و صنايع .
3- ارائه خدمات آموزشي در سطح دانشگاهها ، دبيرستانها و موسسات آموزشي.
4- ارائه طرحهاي پژوهشي به منظور استفاده از منابع اوليه ارزنده موجود در جامعه در جهت افزايش بهرهوري از آنها و جلوگيري از صادرات بيرويه مواد اوليه ارزشمند و تبديل آنها به محصولات واسطهاي كه ارزش اقتصادي بالاتري دارند.
5- ارائه خدمات در كارخانجات پتروشيمي ، پلاستيك ، لاستيك ، رنگ و رزين ، الياف ، صنايع غذايي ، صنايع دارويي، بهداشتي و شويندهها .
6- آمادگي براي ادامه تحصيلات در مقاطع بالاتر براي تامين كادر علمي دانشگاهها و ساير مراكز علمي.
7- كمك به توسعه صنايع دستي كه در سطح گستردهاي در جامعه پراكنده هستند؛ از جمله ساخت رنگهاي بهتر و متنوعتر، بخصوص استفاده از رنگهاي طبيعي موجود در صنعت فرش.
8- استفاده از گياهان دارويي فراواني كه در مملكت موجودند، به منظور استخراج و شناسايي موارد كاربرد اين گياهان به كمك متخصصان داروساز.
هدف از اين دوره تربيت كارشناساني است كه در زمينههاي آموزش در دبيرستان، تربيت كمك پژوهشگر، آماده كردن دانشجويان براي ورودبه دورههاي كارشناسي ارشد و دكتري به منظور تامين كادر آموزشي، پژوهشي مورد نياز دانشگاهها و موسسات تحقيقاتي ، كارشناسان مورد نياز صنايع شيميايي و بينيازي از كارشناسان خارجي بتوانند از عهده برآيند. دوره داراي دو گرايش: شيمي محض ، شيمي كاربردي است. داوطلب بايد در دروس شيمي، فيزيك و رياضي دبيرستان قوي بوده ، علاقه ، انگيزه و روحيه كاوشگري لازم را دارا باشد. دروس به صورت عمومي ، پايه ، الزامي (مشترك بين دو گرايش ) و اختصاصي ارائه ميشود. بعضي دروس الزامي عبارت است از : شيمي آلي ، شيمي تجزيه، شيمي فيزيك، شيمي معدني، معادلات ديفرانسيل. علاوه بر اين دروس 32 واحد درسي در هر گرايش وجود دارد. در شاخه شيمي محض و شيمي كاربردي 20 واحد از اين 32 واحد انتخابي است.
بعضي تواناييهاي فارغالتحصيلان به شرح زير است:
عهدهدار شدن مسووليت هدايت آزمايشگاهها و كمك به امر تدريس شيمي در دانشگاهها ، همكاري در زمينههاي پژوهشي در موسسات ذيربط و دانشگاهها، سرپرستي آزمايشگاههاي كنترل كيفيت مواد اوليه و محصولات در صنايع شيميايي و رفع مشكلات شيميايي صنايع موجود ، ارائه روشهاي بهتر جهت بالا بردن سطح توليد از نظر كيفي و كمي.
با توجه به نياز دانشگاهها به مدرس شيمي، نياز صنايع مختلف شيميايي به پژوهشگر و كمبود متخصص ايراني براي اداره كنترل كيفيت آزمايشگاههاي شيمي صنايع موجود، اهميت اين رشته مشخص ميشود.
امكان ادامه تحصيل در اين رشته تا حد دكتري در داخل و خارج از كشور وجود دارد. برخي از مراكز جذب كارشناسهاي شيمي به شرح زير است:
وزارتخانههاي آموزش و پرورش ، صنايع سنگين ، صنايع و معادن ، فرهنگ و آموزش عالي ، كشاورزي ، نفت و نيز آموزشگاههاي شيمي، صنايع شيميايي و نظاير آنها .
نظر دانشجويان : رشته شيمي از لحاظ محتوا بسيار گسترده و با اكثر صنايع به نحوي مرتبط است، به همين دلايل زمينههاي پژوهش و استخدام بسيار وسيع است.
گرايشهاي مقطع ليسانس:
رشته شيمي در مقطع كارشناسي داراي دو گرايش «محض و كاربردي» ميباشد.
محض و كاربردي عنوان گرايشهاي بعضي از رشتههاي دانشگاهي مثل شيمي و رياضي است اما اين دو گرايش چه تفاوتي با يكديگر دارند؟
دكتر جمشيد مفيدي استاد شيمي دانشگاه تهران در معرفي اين دو گرايش ميگويد:
«در گرايش محض مبناي كار علم شيمي است و دانشجو درباره چهار گرايش اصلي علم شيمي كه عبارتنداز : شيمي آلي ، معدني ، تجزينه و شيمي فيزيك دروسي را مطالعه ميكند. اما در شيمي كاربردي، دروس پايه شيمي كمتر مطالعه ميشود و دانشجو يكسري از دروس مربوط به مهندسي شيمي مثل اصول صنايع شيميايي و تصفيه آب و فاضلاب را ميگذراند.»
دكتر مفيدي در مورد موقعيت شغلي فارغالتحصيلان اين دو گرايش ميگويد:
« فارغالتحصيل شيمي محض در شروع يك فعاليت صنعتي نقش دارد چرا كه او راهكارهاي تئوريك ساخت يك ماده را ارائه ميدهد و سپس يك فارغالتحصيل شيمي كاربردي و يا مهندس شيمي طراحي نيمه صنعتي ماده مورد نظر را ارائه ميدهد.»
دكتر پرويز رنجبر رشيدي استاد شيمي دانشگاه تهران نيز در معرفي اين دو گرايش ميگويد:
«تفاوت اين دو گرايش در نحوه نگرش آنها به علم شيمي است چون شيمي كاربردي نگرشي كاربردي به علم شيمي دارد و ميخواهد از آموختههاي شيمي در صنعت استفاده كند و به همين دليل فارغالتصيلان اين گرايش با مفاهيمي كه در صنايع شيمي مطرح است آشنايي بيشتري داشته و بهتر جذب بازار كار ميشوند اما هدف شيمي محض پرورش دانشجوياني است كه كارهاي تحقيقاتي انجام بدهند و با تحصيل در دوره فوقليسانس و دكترا به حل مسائل و ناشناختههاي علمي شيمي بپردازند. از همينرو درسهاي نظري گرايش شيمي محض بيشتر از دروس كاربردي آن است.»
اميد خاكشور دانشجوي كارشناسي ارشد شيمي دانشگاه صنعتي شريف نيز ضمن معرفي اين دو گرايش ميگويد:
«هرچند كه شيمي محض بيشتر به تئوريهاي عميقتر شيمي ميپردازد و شيمي كاربردي با ارائه يكسري واحدهاي كاربردي، ارتباط نزديكتري با صنعت دارد ، اما اين دو گرايش در سطح ليسانس فرق زيادي با يكديگر ندارند و اگر كسي مايل باشد از هر دو گرايش اطلاع داشته باشد، ميتواند در دروس اختياري ، بعضي از واحدهاي اختصاصي گرايش ديگر را انتخاب كند. البته واقعيت اين است كه فارغالتحصيلان شيمي كاربردي راحتتر جذب بازار كار ميشوند كه آن هم بيشتر به خاطر عنوان اين گرايش است تا معلومات فارغالتحصيلان آن!»
آينده شغلي ، بازار كار ، درآمد:
دكتر رفيعي در انتها ميگويد:
«البته بايد گفت اين طور نيست كه هيچ فرصت شغلي براي فارغالتحصيلان اين رشته مهيا نباشد چون تعدادي از فارغالتحصيلان شيمي جذب صنايع شيميايي مختلف مثل صنايع رنگسازي، چرمسازي، پتروشيمي ، موادغذايي، لوازم بهداشتي و آرايشي ميشوند و در بخش آزمايشگاههاي كنترل كيفيت محصولات شيميايي و يا واحد توليد آنها كار ميكنند.»
دكتر جمشيد مفيدي نيز در مورد فرصتهاي شغلي فارغالتحصيلان اين رشته ميگويد:
«من فكر ميكنم كه شيمي جزو معدود رشتههايي است كه فارغالتحصيل آن ميتواند هميشه مشغول به كار باشد. چون هر كارخانهاي كه داير شود، در بخش كنترل كيفيت كالاهاي ساخته شده نياز به يك شيميست دارد و يا در تمام صنايع احتياج به فارغالتحصيلان شيمي داريم تا مواد اوليه را با توجه به استانداردهاي جهاني بررسي كرده و رد يا قبول بكنند.
علاوه بر موارد فوق يك شيميست ميتواند در خانه خود با كمترين امكانات كارگاه كوچكي داير كرده و بعضي از مواد مورد نياز جامعه را توليد كند براي مثال من فردي را ميشناسم كه بعضي از مواد مورد نياز وزارت دفاع را در يك كارگاه كوچك تهيه ميكرد.»
دكتر پرويز رنجبر رشيدي نيز در همين زمينه ميگويد:
«فارغالتحصيلان اين رشته توانايي تغيير و تبديل بر روي مواد خام را دارند و به ياري همين توانايي، تعداد زيادي از فارغالتحصيلان اين رشته كارگاهها يا كارخانههاي شيميايي كوچك يا بزرگ داير كرده و در كار خود نيز موفق بودهاند.
در ضمن فارغالتحصيل شيمي ميتواند در كارگاهها و كارخانههاي تهيه مواد آلي، دارويي ،رنگها ، رزينها و تهيه و ترخيص مواد معدني كار بكند. »
ظرفيت پذيرش كل و گرايش مختلف :
طي سه سال تحصيلي 76 تا 78 بطور متوسط در هر سال 446 نفر دانشجو از گره آزمايشي علوم رياضي و فني و 2772 نفر از گروه علوم تجربي در رشته شيمي پذيرفته شدهاند.
تواناييهاي مورد نياز و قابل توصيه
شيمي يعني حفظ كردن صدها فرمول، عدد و رقم . اين تصور بسياري از دانشآموزان دبيرستاني است . تصوري كه به اعتقاد دكتر جمشيد مفيدي از دبيرستانها نشأت ميگيرد چرا كه حجم مطالب كتاب شيمي دبيرستاني زياد و فرصت تدريس محدود است و به ناچار دبيران و محصلان به جاي درك و استدلال مفاهيم، به سوي مسايل ذهني و حفظي كشيده ميشوند. در حالي كه شيمي تلفيقي از مهارتهاي ذهني و استدلالي است و اگر كسي بخواهد در اين رشته موفق گردد بايد در هر دو زمينه توانمند باشد و حتي ميتوان گفت كه قدرت استدلال بيش از قدرت حافظه در اين رشته اهميت دارد چون حافظه فقط ميتواند به كار سرعت بدهد اما حلال مشكلات نيست.
وي همچنين معتقد است كه دانشجوي اين رشته لازم است در دروس رياضي، شيمي و فيزيك قوي باشد و رشته شيمي را دوست بدارد يعني از مطالعه درس شيمي لذت ببرد و خسته نشود.
«دانشجوي شيمي بايد به شيمي علاقهمند باشد نه اين كه رشته شيمي در فرم انتخاب رشته، انتخاب چهلم و پنجاهم او باشد. همچنين دانشجو بايد مثل مارگيرهاي قديمي كه مار را ميگرفتند و از آن استفاده بهينه ميكردند، شجاع بوده و وسواس نداشته باشد چون بعضي از مواد شيميايي مثل مار خطرناكند اما اگر كسي طرز استفاده از همين مواد را بلد باشد، موادي قابل كنترل و بسيار مفيد هستند.»
وضعيت ادامه تحصيل در مقاطع بالاتر :
رشته شيمي در ايران تا مقطع دكترا تدريس ميشود.
دوره كارشناسي ارشد شيمي دورهاي با گرايشهاي تخصصي در پنج گرايش (شيمي آلي ، شيمي تجزيه ، شيمي معدني ، شيمي فيزيك ، شيمي كاربردي ) است.
دوه دكتراي شيمي نيز پس از دوره كارشناسي ارشد در دو بخش «آموزشي و پژوهشي» ارائه ميگردد.
رشتههاي مشابه و نزديك به اين رشته :
اين رشته داراي واحدهاي مشابه با رشته مهندسي شيمي ميباشد.
وضعيت نياز كشور به اين رشته در حال حاضر:
شهرام سعادت دانشجوي اين رشته نيز با اشاره به اشتغالزايي اين رشته ميگويد:
«شيمي رشتهاي است كه هم براي فارغالتحصيلان شيمي و هم براي افراد مختلف جامعه فرصت شغلي ايجاد ميكند. براي مثال با ايجاد هر شغل در صنعت پتروشيمي حدود بيست شغل در صنايع پايين دستي و وابسته به وجود ميآيد.»
دكتر رفيعي در تاييد اين سخن ميگويد:
«تنها كافي است وضعيت واردات كشور خودمان را بررسي كنيم تا به واقعيت سخن لينوس پاولينگ پي ببريم. چون درحال حاضر كشور ما هر ساله حدود 5 ميليارد دلار صرف خريد 3500 كالاي شيميايي ميكند. يعني ما يك كيلو نفت را 10 سنت ميفروشيم آن وقت يك كيلو از مواد شيميايي را 40 هزار ، 50 هزار و حتي بعضي از داروهاي شيميايي را تا 100 هزار دلار خريداري ميكنيم .
اين در حالي است كه كشور ما به دليل داشتن هيدرو كربنها، منابع معدني و همچنين نيروي انساني متخصص ميتواند كالاهاي شيميايي بسياري را توليد كند. كاري كه چين انجام داد و توانست با كمترين امكانات ، بازار كالاهاي شيميايي دنيا را قبضه كند. »
وي در ادامه ميگويد:
«در ضمن بايد توجه داشت كه خريد كالاهاي شيميايي نه تنها به بودجه كشور فشار سنگيني وارد ميكند بلكه فرصتهاي شغلي صدها فارغالتحصيل رشته شيمي را نيز از بين ميبرد. افرادي كه بايد با استفاده از منابع اوليه كشور به توليد كالاهاي شيميايي بپردازند. »
نكات تكميلي :
رشته شيمي از جمله رشتههايي است كه داوطلبان دو گروه آزمايشي علوم رياضي و فني و علوم تجربي ميتوانند آن را انتخاب كنند. البته مواد امتحاني و ضرايب اين رشته در هر گروه آزمايشي متفاوت است و دانشگاهها نيز براي داوطلبان هر گروه ظرفيت پذيرش ويژهاي در نظر گرفتهاند.
__________________
مرا سر نهان گر شود زير سنگ -- از آن به كه نامم بر آيد به ننگ
به نام نكو گر بميــرم رواست -- مرا نام بايد كه تن مرگ راست
|
|
جای تبلیغات شما اینجا خالیست با ما تماس بگیرید
|
|

02-26-2010
|
 |
|
|
تاریخ عضویت: Aug 2009
نوشته ها: 16,247
سپاسها: : 9,677
9,666 سپاس در 4,139 نوشته ایشان در یکماه اخیر
|
|
 مطالب مفید و مهم شیمی معدنی
مطالب مفید و مهم شیمی معدنی
شیمی معدنی
شیمی معدنی شاخهای از دانش شیمی است که با کانیها (مواد معدنی) و خواص آنها سروکار دارد.
شیمی معدنی شاخه بزرگی از علم شیمی است که بطور کلی شامل بررسی، تحلیل و تفسیر نظریههای خواص و واکنشهای تمام عناصر و ترکیبات آنها بجز هیدروکربنها و اغلب مشتقات آنهاست.
به عبارت دیگر میتوان چنین اظهار نظر کرد که شیمی معدنی کلیه موادی که از جمله ترکیبات کربن نباشند، به استثنای اکسیدهای کربن و دی سولفید کربن را دربر میگیرد.
نگاه کلی
در شیمی معدنی در مورد گستره وسیعی از موضوعات از جمله: ساختمان اتمی، بلورنگاری (کریستالوگرافی)، انواع پیوندهای شیمیایی اعم از پیوندهای کووالانسی، یونی، هیدروژنی و ...، ترکیبات کوئوردیناسیون و نظریههای مربوطه از جمله نظریه میدان بلور و نظریه اوربیتال مولکولی، واکنشهای اسید و باز، سرامیکها، تقارن مولکولی و انواع بخشهای زیرطبقه الکتروشیمی (برقکافت، باطری، خوردگی، نیمه رسانایی و غیره) بحث میشود.
در باب اهمیت شیمی معدنی، ساندرسن چنین نوشته است:
در واقع بیشترین مباحث علم شیمی را دانش اتمها تشکیل میدهد و کلیه خواص مواد و ترکیبات، به ناچار ناشی از نوع اتمها و روشی است که با توجه به آن، اتمها به یکدیگر میپیوندند و مجموعه تشکیل میدهند و از طرف دیگر کلیه تغییرات شیمیایی متضمن بازآرایی اتمهاست. در این حال شیمی معدنی تنها بخشی از علم شیمی است که با توجه به آن میتوان به صورتی ویژه، در باب مغایرتهای موجود در میان کلیه انواع اتمها بررسی نمود.
طبقه بندی مواد معدنی
در یک مفهوم گسترده، مواد معدنی را میتوان در چهار طبقه تقسیم بندی نمود: عناصر، ترکیبات یونی، ترکیبات مولکولی و جامدات شبکهای یا بسپارها.
عناصر: عناصر دارای ساختارها و خواص بسیار متفاوت هستند. بنابراین میتوانند به یکی از صورتهای زیر باشند:
گازهای اتمی (Kr , Ar) و یا گازهای مولکولی (Latex Error:
{O_2 , H_2})
جامدات مولکولی (Latex Error:
{C_6 , S_8 , P_4})
مولکولها و یا جامدات شبکهای گسترش یافته (الماس، گرافیت)
فلزات جامد (Co , W) و یا مایع (Hg , Ca)
ترکیبات یونی: این ترکیبات در دما و فشار استاندارد همواره جامدند و عبارتاند از:
ترکیبات یونی ساده، مانند NaCl که در آب یا دیگر حلالهای قطبی محلولاند.
اکسیدهای یونی که در آب غیر محلولاند، مانند () و اکسیدهای مختلط همچون اسپنیل (Latex Error:
{MgAl_2O_4})، سیلیکاتهای مختلف مانند Latex Error:
{CaMg(SiO_3)_2} و ...
دیگر هالیدهای دوتایی، کاربیدها، سولفیدها و مواد مشابه. چند مثال عبارتست از: BN , GaAs , SiC , AgCl.
ترکیباتی که دارای یونهای چند اتمی (به اصطلاح کمپلکس) هستند، همچون Latex Error:
{Ni(H_2O)_6{2+} , Co(NH_3)_6{3+} , SiF_6^{2-}} .
ترکیبات مولکولی: این ترکیبات ممکن است جامد، مایع و یا گاز باشند و مثالهای زیر را دربر میگیرند:
ترکیبا دوتایی ساده همچون Latex Error:
{UF_6 , OsO_4 , SO_2 , PF_3} .
ترکیبات پیچیده فلزدار همچون Latex Error:
{RuH(CO_2Me)(PPh_3)_3 , PtCl2(PMe_3)_2} .
ترکیبات آلی فلزی که مشخصا پیوندهای فلز به کربن دارند، مانند Latex Error:
{Zr(Cn_2C_6H_5)_4 , Ni(CO)_4} .
جامدات شبکهای یا بسپارها: نمونههای این مواد شامل بسپارهای متعدد و متنوع معدنی و ابررساناها است. فرمول نمونهای از ترکیبات اخیر Latex Error:
{YBa_2Cu_3O_7} است.
ساختارهای مواد معدنی
ساختار بسیاری از مواد آلی از چهار وجهی مشتق میشود. فراوانی آنها به این دلیل است که در مواد آلی ساده، بیشترین ظرفیت کربن و همچون بیشتر عناصر دیگری (به استثنای هیدروژن) که معمولاً به کربن پیوند میشوند، چهار است. اما اجسام معدنی وضعیت ساختاری بسیار پیچیدهای دارند، زیرا اتمها ممکن است خیلی بیشتر از چهار پیوند تشکیل دهند. بنابراین، در مواد معدنی اینکه اتمها پنج، شش، هفت، هشت و تعداد بیشتری پیوند تشکیل دهند، امری عادی است. پس تنوع شکل هندسی در مواد معدنی خیلی بیشتر از مواد آلی است.
ساختار مواد معدنی اغلب بر اساس تعدادی از وجیهای با نظم کمتر، نظیر دو هرمی با قاعده مثلث، منشور سه ضلعی و غیره و همچنین بر اساس شکلهای باز چند وجیهای منتظم یا غیر منتظم که در آنها یک یا چند راس حذف شده است، نیز مشاهده میشود.
انواع واکنشهای مواد معدنی
در بیشتر واکنشهای آلی میتوانیم در مورد مکانیسمی که واکنش از طریق آن انجام میشود، بحث و بررسی کنیم، در صورتی که برای بسیاری از واکنشهای معدنی فهم دقیق مکانیسم غیر ممکن یا غیر ضروری است.
رابطه شیمی فیزیک و شیمی معدنی
در توجیه موجودیت مواد معدنی و در توصیف رفتار آنها، به استفاده از جنبههای خاصی از شیمی فیزیک، بخصوص ترمودینامیک، ساختارهای الکترونی اتمها، نظریههای تشکیل پیوند در مولکولها، سینتیک واکنش و خواص فیزیکی مواد نیاز داریم. بنابراین با استفاده از شیمی فیزیک میتوان به ساختار اتمی و مولکولی، تشکیل پیوند شیمیایی و دیگر اصول لازم برای درک ساختار و خواص مواد معدنی پرداخت.
__________________
زمستان نیز رفت اما بهارانی نمی بینم
بر این تکرارِ در تکرار پایانی نمی بینم
به دنبال خودم چون گردبادی خسته می گردم
ولی از خویش جز گَردی به دامانی نمی بینم
چه بر ما رفته است ای عمر؟ ای یاقوت بی قیمت!
که غیر از مرگ، گردن بند ارزانی نمی بینم
زمین از دلبران خالی است یا من چشم ودل سیرم؟
که می گردم ولی زلف پریشانی نمی بینم
خدایا عشق درمانی به غیر از مرگ می خواهد
که من می میرم از این درد و درمانی نمی بینم
استاد فاضل نظری |

02-26-2010
|
 |
|
|
تاریخ عضویت: Aug 2009
نوشته ها: 16,247
سپاسها: : 9,677
9,666 سپاس در 4,139 نوشته ایشان در یکماه اخیر
|
|
 شیمی سیمان
شیمی سیمان
شیمی سیمان
سيمان : هر يك از انواع خاص سيمان نسبتهاي مختلفي از سيستم سه تايي SiO2 _ AlO2 _ CaO مي باشد.
سيمان به عنوان چسب:
سيمان به عنوان چسب براي چسباندن خرده ها و ذرات چوب سالها مورد استفاده بوده است. با اين ماده و با استفاده از خاك اره بلوكهايي براي تهيه ي ديوارهاي داخلي منازل تهيه مي شد. در اروپا قطعاتي مركب از چوب و پشم تهيه مي شد كه به دليل دارا بودن دوام زياد و هدايت گرمايي كم كاربرد وسيعي در ساخت پوشش روي سقف ساختمانها داشت.تلاش هاي اوليه براي توليد تخته هاي ساخته شده از سيمان و خرده چوب به دليل سنگيني زياد و استحكام كم محصول و به ويژه مقاومت كم ان در برابر ضربه چندان موفقيت آميز نبود. در تهيه ي چند سازه هاي چوب _ سيمان بايستي در انتخاب گونه ي چوب مناسب دقت شود تا از تخريب شيميايي سيمان (مسموم شدن سيمان ) جلوگيري شود. به دليل مقدار و نوع قند ها ٬ همي سلولزها و تركيبات فنولي موجود در چوب اغلب گونه ها گاهي اوقات سيمان خودش را نمي گيرد.در اينجا بايد پرورده شدن (سفت شدن ) تحت فشار انجام گيرد.از آنجا كه پرورده شدن سيمان فرايند بسيار كندي است لازم است قطعات ساخته شده را به صورت متصل به گيره به مدت 6 تا 8 ساعت در اتاق هاي گرم 70 تا 80 درجه ي سانتي گراد نگه داشت. همين موضوع فرايند توليد را كند مي كند و قيمت فراورده را بالا مي برد. گرچه با استفاده از چسب هاي سيماني تخته هاي سنگيني توليد مي شود با استفاده از سيمان پورتلند تخته هايي توليد مي شود كه پايداري ابعادي زيادي دارند. اين تخته ها بسيار پردوام بوده و تقريبا نسوزمي باشند.
سيمان پرتلند : اين نوع سيمان مهمترين نوع سيمان از نظر توليد و مصرف به شمار مي رود. اين ماده از كلينكر و افزودني هاي گچ يا آنيدريت تشكيل شده است.مواد اوليه ي مورد استفاده در توليد كلينكرهاي سيمان پرتلند عبارتند از : مارل آهكي (مخلوط طبيعي سنگ آهك و رس ) يا مخلوط سنگ آهك يا نرم آهك با رس.
اجزاء كلينكر سيمان پرتلند : وجود تري كلسيم سيليكات در سيمان پرتلند اين ماده را از خواص مطلوبي نظير سخت شدن سريع و استحكام بالا بهره مند مي سازد. به همين دليل در توليد كلينكرهاي سيمان پرتلند اطمينان از مقدار تري كلسيم سيليكات تا بيشترين حد ممكن حائز اهميت است. تنظيم دقيق مقدار آهك از اهميت فراواني برخوردار است. طبق نظر اچ كوهل حداكثر مقدار آهكي كه مي تواند با SiO2 ٫ Al2 O3 و Fe2 O3 تركيب شود با استفاده از فرمول زير محاسبه مي شود:
CaOMax = 2.8x SiO2 + 1.1xAl2 O3 + 0.7x Fe2 O3
وقتي مقدار آهك از مقدار مجاز بالاتر باشد در كلينكر آهك آزاد وجود خواهد داشت. Ca( OH)2 يا Mg(OH)2 كه در اثر هيدراته شدن آهك آزاد (CaO يا MgO) ايجاد مي شود فضاي بيشتري نسبت به اكسيد اوليه اشغال مي كند. پديده ي معروف به انفجار آهكي يا انفجار منيزيايي ناشي از حضور همين كلوخه هاي درشت بلورين CaO يا MgO است زيرا واكنش با آب بسيار آهسته انجام مي گيرد و پس از سخت شدن سيمان نيز ادامه مي يابد. در نتيجه مقدار اهك اضافه شده هميشه كمتر از مقدار محاسبه شده مي باشد.
توليد سيمان پرتلند: براي توليد كلينكر از روشهاي مختلفي استفاده مي شود: در روش تر مواد آغازين به صورت تر آسياب مي شوند تا يك دوغاب خام به وجود ايد سپس اين دوغاب در كوره ي دوار خشك و پخته مي شود در اين روش امكان تامين ساده و دقيق مقدار اجزاء تركيب وجود دارد و مرحله ي آسياب به انرژي كمي نياز دارد. در صورتي كه در مرحله ي پخت بعدي به دليل مقدار آبي كه بايد تبخير شود انرژي بيشتري مصر ف خواهد شد. استفاده از روش تر صرفا در مواردي كه مقدار آب موجود در مواد آغازين بيش از بيست در صد و يا انجام عمليات تر اجتناب ناپذير باشد. در روش نيمه تر آب دوغاب خام كه به صورت تر تهيه شده به كمك صافي فشار (----- پرس ) خارج مي شود خمير حاصل به شكل گندله پرس شده و به همين صورت در كوره ي دوار پخته مي شود. در روش نيمه خشك كه متفاوت از روش نيمه تر است مواد آغازين به صورت خشك آسياب و مخلوط مي شوند. سپس خوراك خام همگن شده ي حاصله به كمك آب و برروي ميز گرانول سازي به شكل گندله تبديل مي شود.در روش خشك مواد آغازين به صورت خشك آسياب و مخلوط مي شوند تا خوراك خام به دست آيد مواد در حال آسياب شدن به كمك گازهاي داغ خروجي پخت خشك مي شوند به طوري كه مقدار رطوبت باقي مانده كمتر از يك در صد شود و بعد از آن به كوره ي پخت انتقال داده مي شوند.در تمام روشهاي فوق پخت مواد اوليه در دماي حدود 1450 درجه ي سانتي گراد و معمولا در كوره هاي دوار انجام مي شود. در كوره هاي دوارخوراك خام توسط گازهاي داغ خروجي پيش گرم مي شود با استفاده از پيش گرم هاي ويژه (پيش گرم كنهاي مشبك و پيش گرمكنهاي سيكلوني) بازيابي گرما با كارايي بيشتري صورت مي گيرد. و اما كوره هاي استوانه اي صرفا براي كارخانه هاي خيلي كوچك (كمتر از 300 تن در روز )اقتصادي هستند.نهايتا پس از گذشتن از مراحل فوق كلينكر به دست آمده آسياب مي شود. قبل از آسياب كردن تا 6.5 در صد گچ ( 2H2 O CaSO4 ) يا آنيدريت ( CaSO4 ) به كلينكر اضافه مي شود.
كاربردهاي سيمان پرتلند: اين سيمان در صنايع ساختماني براي توليد بتون همراه با موادي مانند قلوه سنگ ماسه و مواد انبساط يافته و نيز به همراه تقويت كننده ي فولادي (آرماتور) به عنوان بتون مسلح و همچنين به عنوان اتصال دهنده ي آجرها و بلوك هاي ساختماني ديگر به طور گسترده مورد استفاده قرار مي گيرد.
__________________
زمستان نیز رفت اما بهارانی نمی بینم
بر این تکرارِ در تکرار پایانی نمی بینم
به دنبال خودم چون گردبادی خسته می گردم
ولی از خویش جز گَردی به دامانی نمی بینم
چه بر ما رفته است ای عمر؟ ای یاقوت بی قیمت!
که غیر از مرگ، گردن بند ارزانی نمی بینم
زمین از دلبران خالی است یا من چشم ودل سیرم؟
که می گردم ولی زلف پریشانی نمی بینم
خدایا عشق درمانی به غیر از مرگ می خواهد
که من می میرم از این درد و درمانی نمی بینم
استاد فاضل نظری |

02-26-2010
|
 |
|
|
تاریخ عضویت: Aug 2009
نوشته ها: 16,247
سپاسها: : 9,677
9,666 سپاس در 4,139 نوشته ایشان در یکماه اخیر
|
|
 کود کامل
کود کامل
کود کامل
به طور كلي هر ماده معدني يا آلي كه عناصر مورد نياز گياه را از نظر كمي و كيفي تأمين كند و باعث
بهبود وضعيت گياه از لحاظ رشد، عملكرد و مقاومت به بيماري ها شود، كود ناميده مي شود.
كودها به دو دسته اصلي تقسيم مي شود.
الف- كودهاي شيميايي يا معدني
ب- كودهاي آلي و بيولوژيك
الف- كودهاي شيميايي يا معدني
اين دسته از كودها شامل كودهاي ازته، كودهاي فسفاته، كود كامل ماكرو، كودهاي گوگردي و كودهاي
ريز مغذي و... مي شود.
انواع كودهاي معدني در شكل ١ ارائه شده است.
ب- كودهاي آلي يا بيولوژيك
اين دسته از كودها شامل كودهاي حيواني و صنعتي، كود سبز و كود بيولوژيك مي باشد.
كود مورد بررسي در اين گزارش كود كامل ماكرو است كه طبق تعاريف د ر دسته اول يعني كودهاي شيميايي و معدني قرار مي گيرد.
كود كامل به صورت جامد •
كود كامل ماكرو از مهمترين كودهاي توليد داخل كشور است كه داراي سه عنصر اصلي ازت، فسفر و نيز پتاسيم است و تحت عنوان NPK شناخته مي شود . بعضاً در تركيب اين كود از تركيبات روي نيز به ميزان بسيار كم استفاده مي شود. اين كود مصرف عمده و فراواني در بخش كشاور زي داشته و به صورت گرانول به بازار عرضه مي گردد. استفاده از كود ماكرو در مقايسه با كودهاي ازته، فسفر و پتاسيم سبب استفاده بهينه از خاك مي شود.
طبق اطلاعات گرفته شده از شركت خدمات حمايتي كشاورزي كه وظيفه تأمين و توزيع كود كشور را بر عهده دارد ، كود كامل ماكرو مورد استفاده در اراضي كشاورزي كشور محتوي ١٥ درصد ازت، ٨ درصد فسفر و بعضاً شامل ١ تا ٢ درصد روي نيز مي باشد.
موارد كاربرد
انسان براي تأمين غذا كه مهمترين نياز اوست مي بايست از تمامي عوامل مؤثر در تهيه آن استفاده نمايد.
با توجه به رابطه مستقيم مواد غذايي با بخش كشاورزي و همچنين با توجه به روند روز افزون جمعيت جهاني، اين بخش بايد مورد توجه ويژه اي قرار گيرد ، تا با افزايش بهره وري از طريق استفاده بهينه از نهاده هاي كشاورزي از جمله كودهاي شيميايي مواد غذايي مناسب و كافي تهيه شود.
بطور كلي عوامل متعددي نظير آب، كود، حاصلخيزي خاك و دفع آفات در ميزان توليدات كشاورزي دخيل هستند. اما در سال ١٩٩٨ در بيانيه جهاني غذا (WFS)حاصلخيزي خاك به عنوان مهمترين عامل كليدي در برقراري امنيت غذايي و كشاورزي پايدار ذكر شده است.
از طرف ديگر مهمترين عامل در حاصلخيزي خاك، كود دهي مي باشد. به طوريكه مطالعات انجام شده طي سه دهه گذشته بيانگر آن است كه ٣٣ الي ٦٠ درصد افزايش توليدات كشاورزي مرهون مصرف كود در زمين هاي كشاورزي بوده است.
به عبارت ديگر كاربرد اصلي كود كامل ماكرو همچون ساير كودهاي شيميايي تأمين عناصر غذايي خاك به منظور تأمين نياز غذايي گياهان جهت حداكثر بهره وري از خاك است.
كود كامل ماكرو هم در زمين هاي زراعي و هم در زمين هاي باغباني و نيز اراضي شور مورد استفاده قرار مي گيرد.
كود كامل مورد استفاده در زمين هاي زراعي بيش از ٩٥ درصد مصرف كود كامل را به خود اختصاص مي دهد. كود كامل مورد استفاده در اين زمينه به صورت گرانول توليد و مصرف م ي شود. اين كود براي تمام محصولات كشاورزي مناسب مي باشد ولي لازم است قبل از كشت با استفاده از عميق كاري و يا شخم زمين در محل هاي علامت گذاري شده زير خاك قرار گيرند.
در باغباني و اراضي شور نيز كود كامل ماكرو مورد استفاده قرار مي گيرد. اما ترجيحاً توصيه براي مصرف اين كود بايستي براساس آزمون خاك صورت گيرد . اين كود در مرحله قبل از كاشت درخت در چاله غرس نهال و يا در اوايل فصل به عنوان كود پايه مورد استفاده قرار مي گيرد.
همچنين اين كود در درختاني كه مشكل زرد برگي مشابه علائم كمبود ازت و روي دارند نيز مورد استفاده قرار مي گيرد.
علاوه بر آن اين كود براي محصولاتي كه نياز به پتاسيم بالا دارند ، نيز مورد استفاده قرار مي گيرد . مانند محصولات جاليزي به عنوان كود پايه در زمان كاشت و يا در مرحله خاك دهي مناسب مي باشد.
كود كامل ماكرو در خا ك هايي كه ميزان فسفر و پتاسيم آن بالاست، مورد استفاده قرار نمي گيرد. در بعضي موارد نيز اين كود در سيستم آبياري تزريق شده و به همراه آب به خاك داده مي شود.
با توجه به عدم وجود يون كلر در اين كود م ي توان از آن در مزارعي كه احتمال وجود يون كلر بالا به دليل شوري وجود دارد نيز استفاده نمود.
در كشت انواع صيفي و سبزي نيز اين كود م ي تواند هم به صورت تقسيط و هم قبل از كاشت و هم به شكل نواري با جايگزيني عمقي مصرف گردد.
يكي از نكات بسيار مهم در بكار گيري كودهاي ماكرو كنترل كيفيت آنها پيش از مصرف است . به طور كلي كودهاي توليد شده توسط بخش خصوصي و پتروشيمي ها و همچنين كودهاي وارداتي مستمرا تحت كنترل كيفي و آزمايشگاهي قرار مي گيرند و در صورت غير استاندارد بودن از توزيع آنها جلوگيري مي شود. اين امر بدين صورت انج ام مي شود كه كودهاي وارداتي توسط نمايندگي هاي بنادر مطابق روش هاي استا ندارد نمونه برداري شده و براي شركت خدمات حمايتي جهت آزمايش و تائيد فرستاده مي شود . بخش كنترل كيفي امور كود نيز كودهاي ارسالي را از نظر ظاهري بررسي و در صورت تاييد به آزمايشگاه ارسال مي شود.
كودهاي توليدي بخش خصوصي و پتروشيمي ها نيز توسط شعب شركت در مناطق نمونه برداري شده و همانند نمونه هاي وارداتي به بخش كنترل كيفيت ارسال مي شود . به جز عناصر موثر كه مي بايست در كودهاي شيميايي در حد استاندارد باشد، عناصر سرب و كادميوم عناصر مضري هستند كه م ي بايست ميزان آنها زير حد تعيين شده باشند.
٣-فرايند توليد كود كامل
فرايند توليد كود كامل به صورت جامد در واقع شامل يك فرايند Mixingو گرانول سازي است و واحدهاي موجود توليد كننده اين نوع كود در جهان از همين روش جهت توليد كود كامل گرانوله شامل هر سه عنصر NPK استفاده مي كنند.
در فرايند توليد NPK ابتدا مواد اوليه يعني سولفات آمونيوم، سولفات پتاسيم و فسفات آمونيوم توسط آسياب به ذرات ريز تبديل مي شوند. بعد از آسياب مواد با نسبتهاي تعيين شده مطابق فرمولاسيون كود، توزين شده و از طريق قيف هاي خوراك دهنده وارد سيستم مي شوند.
در مرحله اول فرايند مواد درون مخازن استوانه اي همزن دار با يكديگر مخلوط مي شوند. پس از اختلاط توسط سيستم هاي انتقال دهنده به بخش گرانول سازي منتقل مي شوند.
در بخش گرانول سازي مخلوط در دستگاههاي گرانول ساز گرم مي شوند. حرارت سبب ذوب نسبي تركيبات و چسبندگي آنها مي شود. با چرخش همزن ها گرانول ها در سايز هاي مختلف شكل مي گيرند.
در مرحله بعد گرانول ها وارد سيستم خشك كن مي شوند. با استفاده از هواي سرد گرانول ها تشيكل شده و سايزشان تثبيت مي شود.
در مرحله آخر نيز گرانولها الك شده و سايز بندي مي شود و پس از آن توسط تسمه نقاله وارد قسمت بسته بندي مي گردد. نهايتا در اين بخش كود گرانوله درون كيسه (عمدتا ٥٠ كيلوگرمي) بسته بندي شده و قابل عرضه به بازار خواهد بود.
منبع: جزوات اداره صنایع
__________________
زمستان نیز رفت اما بهارانی نمی بینم
بر این تکرارِ در تکرار پایانی نمی بینم
به دنبال خودم چون گردبادی خسته می گردم
ولی از خویش جز گَردی به دامانی نمی بینم
چه بر ما رفته است ای عمر؟ ای یاقوت بی قیمت!
که غیر از مرگ، گردن بند ارزانی نمی بینم
زمین از دلبران خالی است یا من چشم ودل سیرم؟
که می گردم ولی زلف پریشانی نمی بینم
خدایا عشق درمانی به غیر از مرگ می خواهد
که من می میرم از این درد و درمانی نمی بینم
استاد فاضل نظری |

02-26-2010
|
 |
|
|
تاریخ عضویت: Aug 2009
نوشته ها: 16,247
سپاسها: : 9,677
9,666 سپاس در 4,139 نوشته ایشان در یکماه اخیر
|
|
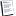 آزمايش تامسون ( محاسبه نسبت بار به جرم الكترون )
آزمايش تامسون ( محاسبه نسبت بار به جرم الكترون )
آزمايش تامسون ( محاسبه نسبت بار به جرم الكترون )
در آزمايش تامسون از اثر ميدان الكتريكي و ميدان مغناطيسي استفاده شده است. دستگاهي كه در اين آزمايش مورد استفاده قرار گرفته است از قسمتهاي زير تشكيل شده است:
الف ) اطاق يونش كه در حقيقت چشمه تهيه الكترون با سرعت معين مي باشد بين كاتد و آند قرار گرفته است. در اين قسمت در اثر تخليه الكتريكي درون گاز ذرات كاتدي ( الكترون ) بوجود آمده بطرف قطب مثبت حركت مي كنند و با سرعت معيني از منفذي كه روي آند تعبيه شده گذشته وارد قسمت دوم مي شود. اگر بار الكتريكي q تحت تاثير يك ميدان الكتريكي بشدت E قرار گيرد، نيروييكه از طرف ميدان بر اين بار الكتريكي وارد مي شود برابر است با:
F= q.E
در آزمايش تامسون چون ذرات الكترون مي باشند q = -e بنابراين:
F= -eE
از طرف ديگر چون شدت ميدان E در جهت پتانسيلهاي نزولي يعني از قطب مثبت بطرف قطب منفي است بنابراين جهت نيرويF در خلاف جهت يعني از قطب منفي بطرف قطب مثبت مي باشد. اگرx فاصله بين آند و كاتد باشد كار نيروي F در اين فاصله برابر است با تغييرات انرژي جنبشي ذرات . از آنجاييكه كار انجام شده در اين فاصله برابراست با مقدار بار ذره در اختلاف پتانسيل موجود بين كاتد وآند بنابراين خواهيم داشت
ev0 =½m0v2
كه در آن v0 اختلاف پتانسيل بين كاتد و آند e بار الكترون v سرعت الكترون و m0 جرم آن مي باشد. بديهي است اگر v0 زياد نباشد يعني تا حدود هزار ولت رابطه فوق صدق مي كند يعني سرعت الكترون مقداري خواهد بود كه مي توان از تغييرات جرم آن صرفنظ نمود . بنابراين سرعت الكترون در لحظه عبور از آند بسمت قسمت دوم دستگاه برابر است با:
v = √(2e v0/ m0)
ب) قسمت دوم دستگاه كه پرتو الكتروني با سرعت v وارد آن مي شود شامل قسمتهاي زير است :
1- يك خازن مسطح كه از دو جوشن A وB تشكيل شده است اختلاف پتانسيل بين دو جوشن حدود دويست تا سيصد ولت مي باشد اگر پتانسيل بين دو جوشن را به v1 و فاصله دو جوشن را به d نمايش دهيم شدت ميدان الكتريكي درون اين خازن E = v1/d خواهد بود كه در جهت پتانسيلهاي نزولي است.
2- يك آهنربا كه در دو طرف حباب شيشه اي قرار گرفته و در داخل دو جوشن خازن: يك ميدان مغناطيسي با شدت B ايجاد مي نمايد . آهنربا را طوري قرار دهيد كه ميدان مغناطيسي حاصل بر امتداد ox امتداد سرعت - و امتداد oy امتداد ميدان الكتريكي - عمود باشد.
پ) قسمت سوم دستگاه سطح دروني آن به روي سولفيد آغشته شده كه محل برخورد الكترونها را مشخص مي كند.
وقتي الكترو از آند گذشت و وارد قسمت دوم شد اگر دو ميدان الكتريكي و مغناطيسي تاثير ننمايند نيرويي بر آنها وارد نمي شود لذا مسير ذرات يعني پرتو الكتروني مستقيم و در امتداد ox امتداد سرعت ) خواهد بود و در مركز پرده حساس p يعني نقطه p0 اثر نوراني ظاهر مي سازد.
اگر بين دو جوشن خازن اختلاف پتانسيلv1 را برقرار كنيم شدت ميدان الكتريكي داراي مقدار معين E خواهد بود و نيروي وارد از طرف چنين ميداني بر الكترون برابر است با FE = e E اين نيرو در امتداد oy و در خلاف جهت ميدان يعني از بالا به پايين است.
ميدان مغناطيسي B را طوري قرار مي دهند كه برسرعتv عمود باشد . الكترون در عين حال در ميدان مغناطيسي هم قرار مي گيرد و نيرويي از طرف اين ميدان بر آن وارد مي شود كه عمود بر سرعت و بر ميدان خواهد بود . اگر اين نيرو را بصورت حاصلضرب برداري نشان دهيم برابر است با:
FM = q.(VXB)
در اينجا q = e پس:
FM = q.(VXB)
و مقدار عددي اين نيرو مساوي است با F = e v B زيرا ميدان B بر سرعت v عمود است يعني زاويه بين آنها 90 درجه و سينوس آن برابر واحد است. اگر ميدان B عمود بر صفحه تصوير و جهت آن بجلوي صفحه تصوير باشد امتداد و جهت نيروي FM در جهت oy يعني در خلاف جهت FE خواهد بود. حال ميدان مغناطيسي B را طوري تنظيم مي نمايند كهFE = FM گردد و اين دو نيرو همديگر را خنثي نمايند. اين حالت وقتي دست مي دهد كه اثر پرتو الكتروني روي پرده بي تغيير بماند پس در اين صورت خواهيم داشت:
FM = FE
e.v.B = e E
v = E/ B
چون مقدار E و B معلوم است لذا از اين رابطه مقدار سرعت الكترون در لحظه ورودي به خازن بدست مي ايد . حال كه سرعت الكترون بدست آمد ميدان مغناطيسي B را حذف مي كنيم تا ميدان الكتريكي به تنهاي بر الكترون تاثير نمايد . از آنجاييكه در جهت ox نيرويي بر الكترون وارد نمي شود و فقط نيروي FE بطور دائم آنرا بطرف پايين مي كشد لذا حركت الكترون در داخل خازن مشابه حركت پرتابي يك گلوله در امتداد افقي مي باشد و چون سرعت الكترون را نسبتا كوچك در نظر مي گيريم معادلات حركت الكترون ( پرتو الكتروني ) در دو جهت ox و oy معادلات ديفرانسيل بوده و عبارت خواهد بود از
m0(d2x /dt2)/span>=0 در امتداox
m0d2y /dt2)=e. E در امتداoy
با توجه به اينكه مبدا حركت را نقطه ورود به خازن فرض مي كنيم اگر از معادلات فوق انتگرال بگيريم خواهيم داشت:
y=(1/2)(e.E)t2/m0
x=v.t
معادلات فوق نشان مي دهد كه مسير حركت يك سهمي است و مقدار انحراف پرتو الكتروني از امتداد اوليه (ox ) در نقطه خروج از خازن مقدار y در اين لحظه خواهد بود . اگرطول خازن را به L نمايش دهيم x = L زمان لازم براي سيدن به انتهاي خازن عبارت خواهد بود از t = L / v اگر اين مقدار t را در معادله y قرار دهيم مقدار انحراف در لحظه خروج از خازن به دست مي آيد:
Y = ½ e( E/m0) ( L/ v )2
e/ m0 = ( 2y/ E ) ( v/ L )2
كه در آن v سرعت الكترون كه قبلا بدست آمده است. L و E بترتيب طول خازن و شدت ميدان الكتريكي كه هر دو معلوم است پس اگر مقدار y را اندازه بگيريم بار ويژه يا e/m0 محاسبه مي شود.
پس از خروج الكترون از خازن ديگر هيچ نيرويي بر آن وارد نمي شود بنابراين از آن لحظه به بعد حركت ذره مستقيم الخط خواهد بود و مسير آن مماس بر سهمي در نقطه خروج از خازن است . اگر a فاصله پرده از خازن يعني D P0 باشد مي توانيم بنويسيم:
P0P1 = y + DP0 tgθ
tgθعبارتست از ضريب زاويه مماس بر منحني مسير در نقطه خروج از خازن و بنابراين مقدار يست معلوم پس بايد با اندازه گرفتن فاصله اثر روي پرده( P0 P1)به مقدار y رسيد و در نتيجه مي توانيم e/ m0 را محاسبه نماييم.
مقداري كه در آزمايشات اوليه بدست آمده بود 108×7/1 كولن بر گرم بود مقداريكه امروزه مورد قبول است و دقيقتر از مقدار قبلي است برابر 108×7589/1 كولن بر گرم است.
علاوه بر تامسون، ميليكان نيز از سال 1906 تا 1913 به مدت هفت سال با روشي متفاوت به اندازه گيري بار الكترون پرداخت.
__________________
زمستان نیز رفت اما بهارانی نمی بینم
بر این تکرارِ در تکرار پایانی نمی بینم
به دنبال خودم چون گردبادی خسته می گردم
ولی از خویش جز گَردی به دامانی نمی بینم
چه بر ما رفته است ای عمر؟ ای یاقوت بی قیمت!
که غیر از مرگ، گردن بند ارزانی نمی بینم
زمین از دلبران خالی است یا من چشم ودل سیرم؟
که می گردم ولی زلف پریشانی نمی بینم
خدایا عشق درمانی به غیر از مرگ می خواهد
که من می میرم از این درد و درمانی نمی بینم
استاد فاضل نظری |

02-26-2010
|
 |
|
|
تاریخ عضویت: Aug 2009
نوشته ها: 16,247
سپاسها: : 9,677
9,666 سپاس در 4,139 نوشته ایشان در یکماه اخیر
|
|
 حقيقت امر لايه ازن چيست؟
حقيقت امر لايه ازن چيست؟
حقيقت امر لايه ازن چيست؟
لايه ازون در قسمت شمالي زمين در سال 1980 بين 15تا20 درصد كاهش پيدا كرده است. براي رفع اين مشكل جمعي ازبهترين متخصصان زمين شناسي هر سال براي تحقيق وجستجو دور يكديگر جمع مي شوند .در سال 1992 پروكتيل مونترئال درباره' لايه اوزون مطالعه و تحقيقي داشت كه فهميد بزرگ شدن سوراخ لايه اوزون بستگي به آلودگي هوا و توليد مواد سمّي دارد.در همان سال سازمان ملل متحد و حفاظت از محيط زيست برنامه اي را طرّاحي كرد كه اين برنامه جهت محافظت و حمايت از محيط زيست و مخصوصا لايه اوزون به نام برنامهUNEPطراحي كرد كه اين برنامه جهت جلوگيري از توليد مواد سمّي و مواد شيميايي آلوده كننده،است.مولكولهاي اكسيژن(O2) به اكسيژن اتميك (O) تبديل مي -شوند .اكسيژن اتميك به سرعت با مو لكولهاي بيشتري تركيب شده و به شكل اوزون مي شود .ان پوشش حرارتي كه در سطح بالا رشد كرده و سلامتي لايه اوزون را به خطر انداخته است و اين مورد باعث شده است كه اگر استراتوسفر نباشد ما نتوانيم بدون آن زنده بمانيم . بالاي استراتوسفر مقداري از آلودگي مضّر اشعه مادون بنفش را و همچنين تشعشعاتي از خورشيد (امواج بين 320 تا 240) را كه باعث مي شود لايه اوزون آسيب ببيند و همچنين جان گياهان به خطر بيفتد را جذب ميكند.اشعه مادون بنفش با تابيدن نور مولكولهاي اوزون را ميشكافد ولي اوزون مي تواند تغيير شكل بدهد و عكس العمل زير ازآن حاصل ميشود:
O + O2 è مادون قرمز +O3
O2 + O è O3
همچنين اوزون در اثر عكس العمل زير نابود ميشود :
O3 + O è O2 + O2
عكس العمل دوم با افزايش پيدا كردن ارتفاع آهسته انجام مي شود امّا عكس العمل سوم سريعتر انجام مي شود. دربين همكاري عكس العمل ها تمركز اوزون درحال تعا دل است. دربالاي اتمسفر اكسيژن اتميك هنگا مي كه اشعه مادون بنفش در سطح بالايي است، پيدا مي شود. در اثر حركت استراتوسفر هواي متراكم تري بدست مي آيد وجذب اشعه ي مادون بنفش افزايش مي يابد و سطح اوزون به حد اكثر و تخمينا" km20مي رسد.همراه با تئوري كمپمن يك مشكل نيز وجود داشت كه اين مشكل در سال 1960 تشخيص داده شد وحقيقت اين بود كه اوزون به وسيله عكس العمل 4 آهسته حركت مي كرد و ديده نمي شود. گرم شدن زمين ترميم حفره اوزون را به تعويق مي اندازد دانشمندان هشدار داده اند :پديده گرم شدن زمين مي تواند تلاشها براي ترميم حفره اوزون را كه قرار بود تا سال 2050 انجام گيرد،حدود30سال به تعويق اندازد .اين مو ضوع به رقم پيشرفتهايي است كه باي از رده خارج كردن مواد شيميايي مخرّب اوزون انجام شده است.
طبق گزارشي كاهش فراواني در مصرف گازهاي ساخته دست انسان بنام (كلروفلورو كربن) پديد آمده است .اينها گازهايي هستندكه لايه محافظ زمين را مي خورند .دانشمندان گفتند:اگر كشورها مصمم به دنبال نمودن اين روند باشند ،(حفره داخل لايه اوزون به آغاز به جمع شدن و كوچك شدن خواهد نمودتا اينكه ظرف 50 سال ترميم خواهد شد . ) اين جمع بندي و نتيجه گيري توسط (مجمع بررسي فرايند هاي استراتوسفر و نقش آن در آب و هوا SPARC به عمل آمد .اين مجمع از صد ها كارشناس اقليمي كه دسامبر سال 1999در آرژانتين گرد هم آمدندو در سايه توجهات سازمان هواشناسي جهاني تشكيل جلسه دادند،شكل گرفته است. اين دانشمندان هشدار دادند: حتّي اگر كاهش مصرف گازهايCFC برآورده شود،پديده گرم شدن زمين_كه نتيجه تولييد گازهاي گلخانه اي با وجود كربن به عنوان عنصر اصلي آن است و از سوختهاي سنگواره اي بدست مي آيد _ميتواند محلت ترميم حفره اوزون را چند دهه به تعويق اندازد.به عنوان يك تناقض ، گرم شدن زمين ،جو را در نزديكي سطح زمين حرارت ميدهد اما لايه پاييني (استراتوسفر) يعني جايي را كه اوزون قرار دارد همچنان سرد نگه ميدارد . اين دماهاي پايين به ويژه درزمستان مسبب جمع شدن ابرهاي استراتوسفر در نواحي قطبي ميشود . اين پديده آغازگر واكنشهاي نابود كننده اوزون توسط مولكولهاي كلري استكه توسط كلروفلورو كربن ها آزاد ميشوند. پيش بيني هاي داير بر اين كه حفره اوزون كه بالاي قطب جنوب قرار دارد، به زودي كوچك خواهد شد با آخرين اطلا عات مغايرت دارد كه نشان ميدهد كه اين حفره درحال گسترش است وبه طور بي سابقه اي در چند سال اخير بزرگ شده است
__________________
زمستان نیز رفت اما بهارانی نمی بینم
بر این تکرارِ در تکرار پایانی نمی بینم
به دنبال خودم چون گردبادی خسته می گردم
ولی از خویش جز گَردی به دامانی نمی بینم
چه بر ما رفته است ای عمر؟ ای یاقوت بی قیمت!
که غیر از مرگ، گردن بند ارزانی نمی بینم
زمین از دلبران خالی است یا من چشم ودل سیرم؟
که می گردم ولی زلف پریشانی نمی بینم
خدایا عشق درمانی به غیر از مرگ می خواهد
که من می میرم از این درد و درمانی نمی بینم
استاد فاضل نظری |

02-26-2010
|
 |
|
|
تاریخ عضویت: Aug 2009
نوشته ها: 16,247
سپاسها: : 9,677
9,666 سپاس در 4,139 نوشته ایشان در یکماه اخیر
|
|
 شیشه
شیشه
شیشه
شیشه ، مایعی میباشد که بسیار سرد شده است و در حرارتی پایینتر از نقطه انجماد آن ، در حالت مایع قرار دارد و بطور عمومی ، جسمی است شفاف که نور بخوبی از آن عبور میکند و پشت آن بطور وضوح قابل روئیت میباشد.
شیشه از نظر ساختمان مولکولی در حالت جامد آرایش مولکولی نامنظم دارد. در درجه حرارتهای بالا ، شیشه مثل هر مایع دیگری رفتار میکند. اما با کاهش دما ، گرانروی آن بطور غیر عادی افزایش مییابد و باعث میشود مولکولها نتوانند در آرایشی که لازمه کریستال شدن است، قرار گیرند. به این ترتیب شیشه از نظر ساختمان مولکولی مانند مایعات نامنظم است، ولی این ساختمان غیر منظم ، دیگر متحرک نیست.
شیشه جسمی سخت است که سختی آن در حدود 8 میباشد و همه اجسام بجز الماسهها را خط میاندازد. وزن مخصوص شیشه 2.5 گرم بر سانتیمتر مکعب بوده و بسیار تُرد و شکننده است. شیشه در مقابل تمام مواد شیمیایی حتی اسیدهای قوی و بازها مقاومت کرده و تحت تاثیر خورندگی واقع نمیشود، به همین علت ظرف آزمایشگاهی را از شیشه میسازند. فقط اسید فلوئوریدریک (HF) بر آن اثر داشته و شیشه را در خود حل مینماید.
تاریخچه
شیشه گری ، یکی از قدیمیترین حرفههایی است که بشر بدان اشتغال داشته است. مصریها سازنده اولین اشیای شیشهای بودهاند که ظروف بدست آمده از حفاریهای مصر قدمت 5000 ساله دارد. رومیان نیز در فن شیشه گری مهارت داشتهاند و در این صنعت از سایرین پیشرفتهتر بودند. رونق شیشه سازی در نخستین ادوار تاریخ اسلامی صورت گرفته است، زیرا هنری بود که در مساجد و زیارتگاهها و تزئینات مذهبی جلوه خاصی داشته و مورد استفاده قرار میگرفت.
در ایران نیز ساختن شیشه قدمت چند هزار ساله دارد. و نخستین واحد ماشینی تولید شیشه ساختمانی در ایران در سال 1340 شروع بکار کرد.
ترکیبات سازنده شیشه
اجزای اصلی تشکیل دهنده شیشه
با نگاه به جدول عناصر ، کمتر عنصری را میتوان یافت که از آن شیشه بدست نیاید، ولی سه ماده کربنات دو سود ، سنگ آهک و سیلیس ، مواد اصلی تشکیل دهنده شیشه میباشند. مواد شیشه ساز مورد تایید موسسه استاندارد و تحقیقات صنعتی ایران عبارتند از سیلیس (SiO2) ، دیاکسید بور (B2O3) ، پنتا اکسید فسفر (P2O5) که از هر کدام بتنهایی میتوان شیشه تهیه نمود.
گدازآورها :کربنات سدیم (Na2CO3) ، کربنات پتاسیم (K2CO3) و خرده شیشه ، سیلیکات سدیم و پتاسیم (Na2SiO3 , K2SiO3) که حاصل ترکیب سیلیس با گدازآورها میباشند، در آب حل میشوند و از شفافیت شیشه به تدریج کم میکنند. به همین علت است که اغلب شیشههای مصرف شده در گلخانه پس از چند سال کدر میشوند و نور از آنها بخوبی عبور نمینماید.
تثبیت کنندهها :برای آنکه مقاومت شیشه را در مقابل آب و هوا ثابت کنیم، باید اکسیدهای دو ظرفیتی باریم ، سرب ، کلسیم ، منیزیم و روی به مخلوط اضافه کنیم که به این عناصر ، ثابت کننده میگویند.
تصفیه کنندهها :موجب کاستن حباب هوای موجود در شیشه میشوند و بر دو نوعند:
فیزیکی: سولفات سدیم (Na2SO4) ، کلرات سدیم (NaClO3). با ایجاد حبابهای بزرگ حبابهای کوچک را جذب و از شیشه مذاب خارج میکنند.
شیمیایی: املاح آرسنیک و آنتیموان ترکیباتی ایجاد میکنند که حبابهای کوچک داخل شیشه را از بین میبرند.
تا اینجا به موادی اشاره کردیم که عدم وجودشان ، در مواد اولیه باعث از بین رفتن مرغوبیت کالا میشد. حال به چند ماده دیگر که به نوعی در تولید شیشه سهیم هستند، اشاره میکنیم.
افزودنیها
استفاده از بوراکس به جای اکسید و کربنات سدیم (گدازآور) که در اثر حرارت به Na2O و B2O3 تجزیه میشود و در واقع بجای هر دو ماده عمل میکند.
استفاده از نیترات سدیم NaNo3برای از بین بردن رنگ سبز شیشه (ناشی از اکسید آهن که همراه مواد دیگر وارد کوره میشود).
استفاده از اکسید منگنز که باعث مقاومت بیشتر در مقابل عوامل جوی و شفافتر شدن شیشه میشود.
استفاده از اکسید سرب PH3O4 , PbO به جای CaO برای ساختن شیشههای مرغوب بلور و کریستال که باعث درخشندگی شیشه میشوند.
برای ساختن کریستال مرغوب از اکسید نقره استفاده میکنند.
استفاده از فلدسپار که باعث مقاومت بهتر در مقابل مواد شیمیایی میشود.
برای اینکه شیشه در برابر اسید فلوئوریدریک هم مقاوم باشد، ترکیباتی از فسفات به آن میافزایند.
استفاده از خرده شیشه که به ذوب مواد سرعت بیشتری میدهد.
استفاده از اکسید فلزات برای تهیه شیشههای رنگی.
اکسید سزیم برای جذب اشعه زیر قرمز و اکسید بر برای ازدیاد مقاومت حرارتی مورد استفاده قرار میگیرند.
دو نمونه از عناصر تشکیل دهنده که عمومیت بیشتری دارند، در زیر ذکر میگردد.
ترکیبات(1 اکسید سیلیسیم (SiO2) در حدود 74 تا 80 درصد و بقیه شامل پراکسید سدیم (NaO2) تا 15 درصد و اکسید کلسیم 7 تا 12 درصد اکسید منیزیم 2 تا 4 درصد و 2 درصد هم عناصر دیگر مانند Fe2O3 - MnO - Al2O3 - TiP2 - SiO3.
ترکیبات (2 اکسید سیلیسیم (SiO2) در حدود 73 درصد ، اکسید سدیم 15 درصد ، اکسید کلسیم 5.55 درصد ، اکسید منیزیم 3.6 درصد ، اکسید آلومینیوم 1.5 درصد ، اکسید بور (B2O3) و اکسید پتاسیم( K2O) هر کدام 0.4 درصد ، اکسید آهن (Fe2O3) و اکسید سیلیسیم 6 ظرفیتی SiO3 هر کدام 0.3 درصد.
علاوه بر مواد فوق همیشه مقداری خرده شیشه نیز با این مواد وارد کوره میگردد.
انواع شیشه و کاربرد آنها
شیشه به اشکال مختلف مورد استفاده قرار میگیرد. در ساخت لوازم تزیینی مانند گل ، تابلو و غیره در ساختن ظروف آزمایشگاهی و یا ظروف آشپزخانه مانند لیوان ، بطری و غیره و بالاخره در ساختن شیشههای مسطح که در دو نوع ساده و مشجر عرضه میگردد و مصارف مختلفی دارد که عمده ترین کاربرد آن به عنوان در و پنجره در کارهای ساختمانی است که به شکلهای مختلف اعم از شیشههای شفاف ، نیمه شفاف و رنگی ، جاذب حرارت ، ایمنی ، دوجداره ، سکوریت و... وجود دارد.
همچنین در آینه سازی ، صنایع نشکن ، صنایع یخچال سازی ، میزهای شیشهای ، انواع شیشه رومیزی و تیغه کاری ساختمان کاربرد دارد.
شیشه رنگی
به دو طریق میتوان شیشه رنگی بدست آورد.
1.با افزودن و کم کردن بعضی مواد شیمیایی در مصالح اولیه تهیه شیشه. برای نمونه اکسیدهای مسی به شیشه رنگهای مختلف قرمز میدهد و رنگ آبی پر رنگ بوسیله اکسید کبالت بدست میآید. رنگ زرد با افزودن مقداری اکسید اورانیوم و کادمیوم حاصل می گردد.
2.شیشه سفید را در شیشه مذاب رنگی فرو میکنند تا دو روی آن رنگی شود. شیشههای رنگی در ویترین مغازهها ، نمایشگاهها ، آزمایشگاهها و ساختمانهای صنعتی بکار میروند.
شیشه ضد آتش (پیرکس)
همراه مواد اولیه این شیشهها در مقابل حرارت ، مقاومت زیادی دارند، مقدار زیادی اکسید بوریک بکار میرود و سیلیس آنها از انواع شیشههای معمولی بیشتر است. معمولا از آنها به عنوان ظروف آزمایشگاه و آشپزخانه و یا در جلوی بخاریهای دیواری و اجاقها استفاده مینماید.
شیشه مسطح
این نوع شیشه را با اضافه نمودن توری فلزی در میان شیشه میسازند و بیشتر برای درهای ورودی ، کارگاهها ، موتورخانهها ، آسانسورها و هر جایی که خطر شکستن و فروریختن شیشه وجود دارد، استفاده مینمایند.
شیشه دوجداره (مضاعف)
این نوع شیشهها ، از دو لایه ساده و گاهی رنگی که به موازات یکدیگر قرار گرفتهاند و لبهها یا درزهای آنها هوابندی شده است و فضای بین آنها با مواد خشک کنندهای مانند سیلیکاژل ، پُر و یا در بعضی از موارد بین دو لایه ، خلاء ایجاد میشود. این نوع شیشه که عایق گرما ، سرما و صداست، در بسیاری از ساختمانها مانند فرودگاهها ، هتلها و بیمارستانها بکار میرود.
شیشه سکوریت
در این حالت ، شیشه مجددا تا حدود 700 درجه سانتیگراد حرارت داده و بعد بطور ناگهانی و تحت شرایط خاص و کنترل شدهای سرد میشود. این عمل باعث افزایش مقاومت شیشه (حدود 3 الی 5 برابر) در مقابل ضربه و نیز شوکهای حرارتی میگردد. این شیشهها در صورت شکستن ، به ذرات ریز و مکعب شکل تقسیم میشوند که آسیب رسان نیستند. از این نوع شیشه در ویترین فروشگاهها ، درهای شیشهای و پنجرههای جانبی اتومبیلها استفاده میگردد.
شیشه نشکن
این نوع شیشهها شامل دو یا چند لایه شیشهاند که بوسیله ورقههایی از نایلون شفاف تحت حرارت و فشار به هم متصل میشوند. همچنین بعضی از انواع شیشههای طلقدار به عنوان عایق صوتی ، جاذب حرارت ، کاهنده شفافیت و شیشه ایمنی بکار برده میشوند. وقتی که این شیشهها میشکنند، خاصیت کشسانی نایلون مانع از پخش و پراکندگی ذرات شیشه میگردد.
از جمله کاربردهای این نوع شیشهها در خودروها و ویترین مغازههایی که اشیاء گرانقیمت میفروشند استفاده میگردد. ممکن است شیشه نشکن را از جنس شیشه سکوریت بسازند.
شیشه ضد گلوله
از چند لایه شیشه سکوریت و یا نشکن ، شیشه ضد گلوله میسازند. در هنگام وارد شدن گلوله به داخل شیشه ، از نیروی آن کاسته و در میان شیشه متوقف میگردد.
شیشه انعکاسی (بازتابنده)
در این نوع شیشهها ، یک سطح شیشه با یک پوشش منعکس کننده نور و حرارت از جنس فلز یا اکسید فلزی دارای این خاصیت پوشانده میشود. این نوع شیشهها ، نور خورشید را منعکس میکنند و در کاهش حرارت و درخشندگی نور موثر هستند. اگر در روشنایی روز از بیرون به شیشه انعکاسی نگاه کنیم مشاهده میکینم که تصاویر اطراف را مانند آینه باز میتاباند و اگر از داخل به بیرون نگاه کنیم، شیشه کاملا شفاف خواهد بود. شبها پدیده مذکور برعکس است. یعنی شیشه از خارج شفاف و از داخل مانند آینه است.
این شیشه با منعکس نور خورشید ، حرارت ناشی از تابش نور خورشید را بطور قابل ملاحظهای کاهش میدهد و در نتیجه ، باعث صرفه جویی در هزینههای احداث ، راه اندازی و نگهداری سیستمهای تهویه و تبدیل میشود.
تقسیم بندی شیشههای تجارتی
سیلیس گداخته
سیلیس گداخته یا سیلیس شیشهای به روش تفکافت تتراکلرید سیلیسیم در دمای بالا یا بوسیله گدازش کوارتز یا ماسه خالص ساخته میشود و گاه آن را به اشتباه ، شیشه کوارتزی میخوانند. این ماده ، انبساط کم و نقطه نرمی بالایی دارد که به مقاومت گرمایی زیاد آن کمک میکند و امکان استفاده از آن را در گستره دمایی بالاتر از دیگر شیشهها فراهم میآورد. این شیشه ، اشعه ماوراء بنفش را بخوبی از خود عبور میدهد.
سیلیکاتهای قلیایی
سیلیکاتهای قلیایی تنها شیشههای دو جزئی هستند که از اهمیت تجارتی برخوردارند. ماسه و کربنات سدیم را بسادگی با هم ذوب میکنند و محصولات بدست آمده با گستره ترکیب Na2O.SiO2 تا Na2O.4SiO2 را سیلیکاتهای سدیم میخوانند. سیلیکات محلول کربنات سدیم که به نام شیشه آبی (انحلال پذیر در آب) نیز خوانده میشود، بطور گستردهای در ساخت جعبههایی با کاغذ موجدار و به عنوان چسب کاغذ بکار میرود.
مصرف دیگر آن در ایجاد حالت ضد آتش است. انواع قلیاییتر آن به عنوان شویندههای لباسشویی و مواد کمکی صابونها بکار میرود.
شیشه آهک سوددار
این نوع شیشه %95 کل شیشه تولید شده را تشکیل میدهد و از آن ، برای ساخت تمام انواع بطریها ، شیشه تخت ، پنجره خودروها و سایر پنجرهها ، لیوان و ظروف غذاخوری استفاده میشود. در کیفیت فیزیکی تمام انواع شیشههای تخت ، نظیر همواری و نداشتن موج و پیچ ، بهبود کلی حاصل شده، اما ترکیب شیمیایی تغییر زیادی نکرده است. اصولا ترکیب شیمیایی در گستره زیر قرار میگیرد:
SiO2 از %70 تا %74 ، CaO از %8 تا %13 ،Na2O از %13 تا %18.
فراوردههایی که این نسبتها را دارند، در دماهای نسبتا پایینتری ذوب میشوند. در تولید شیشه بطری ، بخش عمده پیشرفت از نوع مکانیکی است. در هر حال ، تجارت نوشابهها ، سبب ایجاد گرایشی در بین شیشه سازان برای تولید ظروف شیشهای با آلومین و آهک زیاد و قلیائیت کم شده است. این نوع شیشه با دشواری بیشتری ذوب میشود، اما در برابر مواد شیمیایی مقاومتر است.
رنگ شیشه بطریها بدلیل انتخاب بهتر و تخلیص مواد خام و استفاده از سلنیم به عنوان زنگزدا بسیار بهتر از قبل است.
شیشه سربی
با جانشین شدن اکسید سرب به جای اکسید کلسیم در شیشه مذاب ، شیشه سربی بدست میآید. این شیشهها بدلیل برخورداری از ضریب شکست بالا و پراکندگی نور زیاد ، در کارهای نوری از اهمیت بسزایی برخوردارند. تاکنون میزان سرب موجود در شیشه را به %92 نیز رساندهاند.
درخشندگی یک بلور تراش داده شده خوب بدلیل مقدار زیاد سرب در ترکیب آن است. مقدار زیادی از این شیشه برای ساخت حباب لامپهای برق ، لامپهای نئون و رادیوترونها بدلیل مقاومت الکتریکی بالای آنها مورد استفاده قرار میگیرد. این شیشه برای ایجاد حفاظ در برابر پرتوهای اتمی نیز مفید است.
شیشه بوروسیلیکاتی
شیشه بوروسیلیکاتی ، معمولا حاوی حدود 10 تا 20 درصد B2O2 ، حدود 80 تا 85 درصد سیلیس و کمتر از 10 درصد Na2O است. این نوع شیشه دارای ضریب انبساط کم ، مقاومت فوقالعاده زیاد در برابر ضربه ، پایداری عالی در برابر مواد شیمیایی و مقاومت الکتریکی بالاست.
ظروف آزمایشگاهی ساخته شده از این شیشه ، تحت نام تجارتی پیرکس فروخته میشود. با این حال ، در سالهای اخیر نام پیرکس برای اجناس شیشهای بسیاری که ترکیب شیمیایی دیگری دارند (مانند شیشه آلومین _ سیلیکات در ظروف شیشهای مناسب برای پخت و پز) نیز بکار میرود. مصارف دیگر شیشههای بوروسیلیکاتی علاوه بر ظروف آزمایشگاهی عبارت است از واشرها و عایقهای فشار قوی ، خطوط لوله و عدسی تلسکوپها.
شیشههای ویژه
شیشههای رنگی و پوششدار ، کدر ، شفاف ، ایمنی ، شیشه اپتیکی ، شیشه فوتوکرومیکی و سرامیکهای شیشهای ، همه شیشههای ویژه هستند. ترکیب تمامی این شیشهها بر طبق مشخصات محصول نهایی موردنظر تغییر میکند.
الیاف شیشهای
الیاف شیشهای از ترکیبات ویژهای که در برابر شرایط جوی مقاوم هستند، ساخته میشوند. سطح بسیار زیاد این الیاف سبب میشود تا آنها نسبت به همه رطوبت موجود در هوا آسیب پذیر باشند. مقدار سیلیس (حدود %55) و قلیایی موجود در این شیشه پایین است.
__________________
زمستان نیز رفت اما بهارانی نمی بینم
بر این تکرارِ در تکرار پایانی نمی بینم
به دنبال خودم چون گردبادی خسته می گردم
ولی از خویش جز گَردی به دامانی نمی بینم
چه بر ما رفته است ای عمر؟ ای یاقوت بی قیمت!
که غیر از مرگ، گردن بند ارزانی نمی بینم
زمین از دلبران خالی است یا من چشم ودل سیرم؟
که می گردم ولی زلف پریشانی نمی بینم
خدایا عشق درمانی به غیر از مرگ می خواهد
که من می میرم از این درد و درمانی نمی بینم
استاد فاضل نظری |

02-26-2010
|
 |
|
|
تاریخ عضویت: Aug 2009
نوشته ها: 16,247
سپاسها: : 9,677
9,666 سپاس در 4,139 نوشته ایشان در یکماه اخیر
|
|
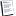 فسفر ٬ فسفر سانس و فلور سانس
فسفر ٬ فسفر سانس و فلور سانس
فسفر ٬ فسفر سانس و فلور سانس
1- تفاوتهای فسفر سانس و فلور سانس چیست؟ توسط :شکیبا
در نتیجه جذب نور توسط برخی اجسام توانایی نشر نور رابه دست می آورند. حال دو حالت وجودارد اگر بعد ازقطع تابش نور جسم بازهم توانایی نشر نوررا داشته باشد فسفر سانس واگر بعد از قطع نور دیگر نشر نور توسط جسم صورت نگیرد این پدیده را فلوئور سانس گویند. فسفر سانس گونه ایی از فلوئورسانس است که درآن اتم ها ومولکول های جذب کننده نور می توانند در حالت های شبه پایدار باقی بمانند.فسفر سانس درآنالیز مواد شیمیایی برای تخمین غلظت مواد بسیار کم شیمیایی استفاده می شود .
2-ویژگی وکاربردهای فسفر سفید توسط :شکیبا
فسفر دارای چندین شکل است که سه آلوتروپ اصلی است . فسفر سفیدp4 به علت کشش زاویه ای درون مولکول ٬ واکنش پذیر ترین نوع فسفر است ودرزیر آب نگهداری می شود زیر آب قطبی وفسفر سفید غیر قطبی درهم حل نمی شوند وهم چنین با هم واکنشی انجام نمی دهند.
فسفر سفید را به کمک ذوب منطقه ایی خالص می کنند .اگر فسفر سفید را دردمای بالا وبه مدت طولانی گرم کنید فسفر قرمز به دست می آید که یک جسم پلیمری است وپایدار است . ازگرم کردن فسفر سفید درزیر فشار بالا فسفر سیاه حاصل می شود. که ساختاری همانند گرافیت دارد .بخار فسفر شاملP4 وP2 می باشد وفسفر سفید خود به خود آتشگیر اما فسفر سیاه عملا اشتعال نا پذیر است فسفر درقلیا هاانحلال ناپذیر اما در اسیدهای اکسید کننده حل می شود.
ترکیب های فسفر کود های شیمیایی با اهمیتی هستند .درکبریت سازی مبارزه با آفت های کشاورزی تهیه شیشه ها وظروف چینی ویژه تهیه آلیاژ ها(فولاد برنز فسفردار )عمل کردن فلز ها شوینده ها ادوات الکتریکی (برای نمونه Gap) در صنایع غذایی ونوشیدنی ها استفاده می شود وفسفات ها از اجزای ضروری برای اندام موجود زنده است .
3- کمی در مورد p4 (فسفر سفید) و هم چنین p4o10 (فسفر(5) اکسید) و p2o5 (دی فسفر پنتا اکسید) توضیح دهید، یعنی ربطشان به هم چیست و چه فرقی با هم دارند، در ضمن در کتاب درسی های ما آمده p4 فسفر سفید است ولی در المپیاد های آمریکا از آن به عنوان فسفر قرمز یاد کرده است!!
اگر فسفر در اکسیژن زیاد به سوزد P4O10 تشکیل می شود. که گردی سفید رنگ است ودر 360 درجه سانتیگراد تصعید می شود. ساختار این مولکول بر مبنای P4 استواراست . ودرهر مولکول از آن 4 اتم فسفر همراه 10 اتم اکسیژن وجود دارد.وبه همین علت فرمول مولکولی به صورت P4O10 نوشته می شود وقابل ساده کردن نیست (مانند مولکولهای آلی نظیر C2H2 ویاC2H4 ویاC2H6 و......) . این مطلب در مورد P4O6نیز صدق می کند.
P4O6 P4O10
قبل از شناسایی مولکول واقعی این ترکیب از فرمول ساده آن P2O5 استفاده می شد .
P4O10 دارای چندین فرم است. و میل ترکیبی شدیدی با آب دارد ویک عامل خشک کننده وآب زدا است . برای تهیه اسیدهای گوناگون فسفریک استفاده می شود.
همان طور که ملاحظه می کنید. فسفر سفید ساختار مولکولی دارد درحالی که فسفر قرمز ساختار پلیمری دارند.
منابع:
فرهنگ شیمی دیوید ویلیام آرتور شارپ
شیمی عمومی جلد دوم چارلز مورتیمر
__________________
زمستان نیز رفت اما بهارانی نمی بینم
بر این تکرارِ در تکرار پایانی نمی بینم
به دنبال خودم چون گردبادی خسته می گردم
ولی از خویش جز گَردی به دامانی نمی بینم
چه بر ما رفته است ای عمر؟ ای یاقوت بی قیمت!
که غیر از مرگ، گردن بند ارزانی نمی بینم
زمین از دلبران خالی است یا من چشم ودل سیرم؟
که می گردم ولی زلف پریشانی نمی بینم
خدایا عشق درمانی به غیر از مرگ می خواهد
که من می میرم از این درد و درمانی نمی بینم
استاد فاضل نظری |

02-26-2010
|
 |
|
|
تاریخ عضویت: Aug 2009
نوشته ها: 16,247
سپاسها: : 9,677
9,666 سپاس در 4,139 نوشته ایشان در یکماه اخیر
|
|
 الماس
الماس
الماس
مقدمه
شاید به زودى تصور متداول درباره الماسها به کلى دگرگون شود. الماسهایى که بخاطر زیبایى ، کمیاب بودن و زمان طولانى تولیدشان ارزش فوق العادهاى داشتند، امروزه در آزمایشگاه و در مدت زمانى حدود یک ساعت بوجود مىآیند. اینکه این دگرگونى چه تأثیرى در صنعت جواهرسازى یا قیمت الماسهاى طبیعى در بازار خواهد داشت هنوز در پردهاى از ابهام است. اما درباره نقش این الماسهاى آزمایشگاهى در تکنولوژى ، شایعههایى برخاسته از مجامع علمى به گوش مىرسد.
بیشتر از هشتاد درصد از الماسهاى معدنى طبیعى به مصارف صنعتى از قبیل ابزارهاى برش یا مواد ساینده براى تراشکارى و پرداخت دیگر سنگهاى قیمتى ، فلزات ، گرانیت و شیشه مىرسند. استفاده از الماس به عنوان نیم رسانا نیز نیازمند شرایط ویژهاى مثل بالاترین درجه خلوص ، بهترین بلورینگى و تعیین اتمها به لحاظ الکتریکى فعال براى ایجاد گذرگاه الکتریکى در وسیله مورد نظر است.
اما تمامى الماسهاى طبیعى بخاطر نقصها ، ناخالصیها و ساختار ضعیفشان براى مصارف الکترونیکى نامناسبند. حتى با اینکه الماسهاى مصنوعى و طبیعى داراى کیفیت جواهرى بسیار ارزشمند هستند، اما ممکن است بخاطر رگههاى ناچیز ناخالصیها براى استفاده به عنوان نیم رسانا مناسب نباشند. در واقع تنها خالصترین این سنگها در کاربردهاى الکترونیکى پرقدرت از سلفونها گرفته تا کامپیوترهاى شخصى و خطوط ارتباطاتى قابل استفادهاند.
دورنماى الماس
میزان ذخیره الماس جهان در سال 1979 بدین شرح میباشد. زئیر 120 ، شوروی (سابق) 250 ، آفریقای جنوبی 72 ، بوستوانا 60 ، نامیبیا 15 ، آنگولا 20 ، سیرالئون 6 و لسوتو 5 میلیون قیراط ذخیره دارند. همچنین میزان الماس تولیدی جهان در سال 1979 بدین شرح میباشد: زئیر 11160 ، شوروی (سابق) 10700 ، آفریقای جنوبی 7640 ، بوتسوانا 3340 ، نامیبیا 1950 ، عتا 1500 ، آنگولا 750 ، ونزوئلا 750 و سیرالئون با 710 قیراط بیشترین تولید الماس جهان را به خود اختصاص دادهاند.
تولید الماس
الماس بطور طبیعى تحت فشارهاى زیاد اعماق زمین و در زمانى طولانى شکل مىگیرد. اما در آزمایشگاه مىتوان به کمک دو فرآیند مجزا در زمانى بسیار کوتاهتر الماس تولید کرد. فرآیند فشار بالا _ دما بالا (HP HT) اساساً تقلیدى است از فرآیند طبیعى شکل گیرى الماس در حالى که فرآیند رسوب گیرى بخار شیمیایى (CVD) دقیقاً خلاف آن عمل مىکند. در واقع CVD بجاى وارد کردن فشار به کربن براى تولید الماس با آزاد گذاشتن اتمهاى کربن به آنها اجازه مىدهد با ملحق شدن به یکدیگر به شکل الماس در آیند.
این دو تکنیک براى اولین بار در دهه 1950 کشف شدند. به گفته باتلر که هفده سال روى تولید الماس با استفاده از تکنیک CVD کار کرده است «از آنجا که پیشگامان تولید الماس بدون فشار بالا در دهه 1950 با تمسخر سایرین از میدان به در شدند. تکنولوژى CVD هنوز دوران کودکىاش را سپرى مىکند.» هر دو فرآیند قادرند با سرعتى خیره کننده الماسهایى با کیفیت جواهر تولید کنند، اما در نهایت این فرآیند CVD است که بخاطر کنترل ساده ناخالصى و اندازه محصول براى تکنولوژیهاى الکترونیکى مناسبترین خواهد بود.
فرآیند CVD با قرار دادن ذره بسیار کوچکى از الماس در خلأ آغاز مىشود. سپس گازهاى هیدروژن و متان به محفظه خلأ جریان مىیابند. در ادامه پلاسماى تشکیل شده باعث شکافته شدن هیدروژن به هیدروژن اتمى مىشود که با متان واکنش مىدهد تا رادیکال متیل و اتمهاى هیدروژن بوجود آیند. رادیکال متیل نیز به ذره الماس مىچسبد تا الماس بزرگ شود. رشد الماس در تکنیک CVD ، فرآیندى خطى است، بنابراین تنها عوامل محدودکننده اندازه محصول در این روش بزرگى ذره ابتدایى و زمان قرار دادن آن در دستگاه است.
به گفته دیوید هلیر (D. Hellier) ، رئیس بخش بازاریابى کمپانى ژمسیس ، «فرآیند HP HT نیز با ذره کوچکى از الماس آغاز مىشود. هر ذره الماس در محفظههاى رشدى به اندازه یک ماشین لباسشویى ، تحت دما و فشار بسیار بالا درون محلولى از گرانیت و کاتالیزورى فلزى غوطهور مىشود. در ادامه تحت شرایط کاملاً کنترل شدهاى این الماس کوچک به تقلید از فرآیند طبیعى ، مولکول به مولکول و لایه به لایه شروع به رشد مىکند.»
گر چه جنرال الکتریک در تولید الماسها به این روش پیشگام است و الماسهاى ساخته شده با تکنیک HP HT را براى مصارف صنعتى به بازار عرضه مىکرد اما تا پیش از آنکه کمپانى ژمسیس با ساده سازى این فرآیند امکان تولید نمونههایى با کیفیت جواهر را فراهم کند، هرگز آن الماسها به عنوان سنگهاى قیمتى به فروش نرسیده بودند.
در واقع الماسهاى زینتى مصنوعى بخش کوچک و در عین حال پر سودى از صنعت الماس را تشکیل مىدهند. این الماسهاى رنگى که در مقایسه با همتاهاى بىرنگ شان فوق العاده کمیاب و در نتیجه بسیار گرانبها ترند با توجه به نوع ناخالصیها در رنگهاى گوناگون از قرمز و صورتى گرفته تا آبى ، سبز و حتى زرد روشن و نارنجى تولید مىشوند. در واقع این الماسها مىتوانند چنان کیفیت بالایى داشته باشند که حتى ماشینهاى ساخته شده براى تشخیص سنگهاى مصنوعى از طبیعى در تفکیکشان از یکدیگر دچار مشکل شوند، همانطور که امروزه برخى از بزرگترین الماس فروشان در صنعت نیز به زحمت از پس آن بر مىآیند.
شباهت فوق العاده نمونه هاى مصنوعى و طبیعى باعث شده است تا تاجران الماس براى تشخیص الماسهاى رنگى مصنوعى از سنگهاى طبیعى دست به دامن آزمایشگاههاى الماس بلژیک و دیگر نقاطى شوند که بطور سنتى عهده دار تجزیه و تحلیل و تأیید الماسها از نظر بزرگى قیراط ، رنگ و شفافیت هستند.
__________________
زمستان نیز رفت اما بهارانی نمی بینم
بر این تکرارِ در تکرار پایانی نمی بینم
به دنبال خودم چون گردبادی خسته می گردم
ولی از خویش جز گَردی به دامانی نمی بینم
چه بر ما رفته است ای عمر؟ ای یاقوت بی قیمت!
که غیر از مرگ، گردن بند ارزانی نمی بینم
زمین از دلبران خالی است یا من چشم ودل سیرم؟
که می گردم ولی زلف پریشانی نمی بینم
خدایا عشق درمانی به غیر از مرگ می خواهد
که من می میرم از این درد و درمانی نمی بینم
استاد فاضل نظری |

02-26-2010
|
 |
|
|
تاریخ عضویت: Aug 2009
نوشته ها: 16,247
سپاسها: : 9,677
9,666 سپاس در 4,139 نوشته ایشان در یکماه اخیر
|
|
 انواع چدن
انواع چدن
انواع چدن
اطلاعات کلی
چدن (cast iron) ، آلیاژی از آهن- کربن و سیلیسیم است که همواره محتوی عناصری در حد جزئی (کمتر از 0.1 درصد) و غالبا عناصر آلیاژی (بیشتر از 0.1 درصد) بوده و به حالت ریختگی یا پس از عملیات حرارتی به کار برده میشود. عناصر آلیاژی برای بهبود کیفیت چدن برای مصارف ویژه به آن افزوده میشود. آلیاژهای چدن در کارهای مهندسی که در آنها چدن معمولی ناپایدار است به کار میروند. اساسا خواص مکانیکی چدن به زمینه ساختاری آن بستگی دارد و مهمترین زمینه ساختار چدنها عبارتند از: فریتی ، پرلیتی ، بینیتی و آستینتی. انتخاب نوع چدن و ترکیب آن براساس خواص و کاربردهای ویژه مربوطه تعیین میشود.
__________________
زمستان نیز رفت اما بهارانی نمی بینم
بر این تکرارِ در تکرار پایانی نمی بینم
به دنبال خودم چون گردبادی خسته می گردم
ولی از خویش جز گَردی به دامانی نمی بینم
چه بر ما رفته است ای عمر؟ ای یاقوت بی قیمت!
که غیر از مرگ، گردن بند ارزانی نمی بینم
زمین از دلبران خالی است یا من چشم ودل سیرم؟
که می گردم ولی زلف پریشانی نمی بینم
خدایا عشق درمانی به غیر از مرگ می خواهد
که من می میرم از این درد و درمانی نمی بینم
استاد فاضل نظری |
|
کاربران در حال دیدن موضوع: 1 نفر (0 عضو و 1 مهمان)
|
|
|
| ابزارهای موضوع |
|
|
| نحوه نمایش |
 حالت خطی حالت خطی
|
 مجوز های ارسال و ویرایش
مجوز های ارسال و ویرایش
|
شما نمیتوانید موضوع جدیدی ارسال کنید
شما امکان ارسال پاسخ را ندارید
شما نمیتوانید فایل پیوست در پست خود ضمیمه کنید
شما نمیتوانید پست های خود را ویرایش کنید
اچ تی ام ال غیر فعال می باشد
|
|
|
اکنون ساعت 12:44 AM برپایه ساعت جهانی (GMT - گرینویچ) +3.5 می باشد.
|





















 حالت خطی
حالت خطی

