
|
|
|||||||
| شیمی در این تالار مباحث و مطالب مرتبط با علم شیمی گذارده خواهد شد |
 |
|
|
ابزارهای موضوع | نحوه نمایش |
|
#1
|
||||
|
||||
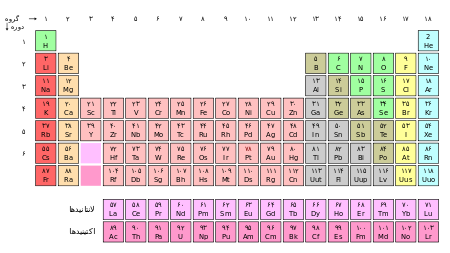
جدول تناوبی ویرایش توسط ROJINAjoON : 10-02-2011 در ساعت 09:04 PM |
| 2 کاربر زیر از ROJINAjoON سپاسگزاری کرده اند برای پست مفیدش: | ||
| جای تبلیغات شما اینجا خالیست با ما تماس بگیرید | |
|
|
|
|
#2
|
||||
|
||||
شناخت عناصرجدول تناوبی
__________________
|
|
#3
|
||||
|
||||
|
نام نرم افزار: نرم افزار جدول تناوبی حجم فایل (MB): 2.30 دریافت نرم افزار: دانلود  توضیح: جدول تناوبی و بدون نیاز به نصب
__________________
|
 |
| کاربران در حال دیدن موضوع: 1 نفر (0 عضو و 1 مهمان) | |
|
|
اکنون ساعت 01:44 AM برپایه ساعت جهانی (GMT - گرینویچ) +3.5 می باشد.





 حالت خطی
حالت خطی

